Общая и неорганическая химия
______________ – частицы адсорбата и адсорбента связываются более прочными силами сцепления за счет возникающего химического взаимодействия, которое приводит к образованию нового химического соединения на поверхности адсорбента
Установите соответствие между понятиями и их определениями
термодинамическая вероятность состояния системы
полная энергия системы, которая складывается из кинетической и потенциальной энергий молекул, атомов, атомных ядер и электронов
стандартная энергия гиббса образования химического соединения
энергия Гиббса реакции образования одного моля этого соединения, находящегося в стандартном состоянии, из соответствующих простых веществ, также находящихся в стандартных состояниях и термодинамически устойчивых при данной температуре фазах и модификациях
внутренняя энергия системы
число микросостояний, с помощью которых осуществляется данное макросостояние
Одним из наиболее распространенных методов ускорения химических реакций является _____________, который осуществляется при помощи веществ, резко увеличивающих скорость реакции, но не расходующихся в результате ее протекания
катализ
цепная реакция
десорбция
адсорбция
Если принять средний уровень энергии молекул исходных веществ в системе равным Е1, а среднюю энергию переходного состояния – Е', то разность Е' – Е1 будет выражать ______________ данной реакции Еа
гомолитический разрыв
энергию активации
состояние активированного комплекса
квантовый выход
Изменение ______________ системы – это сумма изменения внутренней энергии системы в результате превращения исходных веществ в продукты реакции и работы расширения образовавшихся газов
Правило, гласящее, что при постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях, равных стехиометрическим коэффициентам в уравнении реакции, – это
второй закон термодинамики
закон действующих масс
первый закон термодинамики
закон Гесса
______________ энергия Гиббса образования химического соединения – это энергия Гиббса реакции образования одного моля этого соединения, находящегося в стандартном состоянии, из соответствующих простых веществ, также находящихся в стандартных состояниях и термодинамически устойчивых при данной температуре фазах и модификациях
Концентрации газообразных или растворенных веществ А и В в равновесной реакционной смеси называются равновесными концентрациями, а их соотношение СВ/СА выражается константой ______________
Если катализатор и взаимодействующие вещества образуют однофазную систему, катализ называют _____________
открытыми
гомогенным
гетерогенными
закрытыми
Установите соответствие между понятиями и их определениями
химическая термодинамика
изучение скорости и механизма химической реакции
химическое равновесие
состояние системы, при котором скорость прямой реакции равна скорости обратной реакции
химическая кинетика
наука, изучающая переходы химической энергии в другие формы – тепловую, электрическую и т.д.
______________ энергия системы – это полная энергия системы, которая складывается из кинетической и потенциальной энергий молекул, атомов, атомных ядер и электронов
Исключительное значение для развития химии имело установление следующих основных стехиометрических законов
Авогадро
постоянства состава
сохранения массы веществ
единства и борьбы противоположностей
Наименьшую энтропию имеют идеально правильно построенные кристаллы при ______________ нуле
Правило, гласящее, что если на систему, находящуюся в равновесии, оказать внешнее воздействие, то равновесие сместится в том направлении, которое ослабит эффект внешнего воздействия, – это
принцип Ле Шателье
правило Вант-Гоффа
следствие из закона Гесса
уравнение Аррениуса
Определяется числом молекул, одновременным взаимодействием которых осуществляется элементарный акт химического превращения, – _________ реакции
теплота
энергия
энтальпия
молекулярность
Если катализатор и взаимодействующие вещества образуют однофазную систему, катализ называют _____________
Сорбция объемом вещества – это
адсорбция
молекулярность
абсорбция
десорбциия
Внутренняя энергия системы представляет собой ее полную энергию, которая складывается из
кинетической и потенциальной энергий атомных ядер и электронов
кинетической энергии движения системы как целого
потенциальной энергии положения системы в пространстве
кинетической и потенциальной энергий молекул и атомов
Функциональная зависимость константы скорости реакции k от температуры: 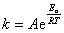 – это
– это
принцип Ле Шателье
следствие из закона Гесса
правило Вант-Гоффа
уравнение Аррениуса
______________ (теплота) образования химического соединения – это изменение энтальпии в процессе образования одного моля этого соединения из простых веществ, устойчивых при данной температуре
Тепловой ______________ химической реакции – это количество теплоты, которое выделяется или поглощается в результате реакций между определенными количествами реагентов при постоянной температуре
Истинная скорость химической реакции vист определяется пределом, к которому стремится отношение ΔC/Δt при 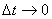 , т.е. производной ______________ по времени:
, т.е. производной ______________ по времени: 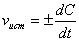
Сумма показателей степеней при концентрациях в кинетическом уравнении реакции (p+q) называется ______________ реакции
квантовым выходом
общим порядком
состоянием активированного комплекса
энергией активации
Вещество, резко увеличивающее скорость реакции, но не расходующееся в результате ее протекания, – это
сорбция
катализатор
сорбит
промотор
Примерами кристаллов, в которых преобладает ионный тип связи, могут быть
NaCl
германий
кремний
KF
алмаз
CaF2
Полная энергия системы, которая складывается из кинетической и потенциальной энергий молекул, атомов, атомных ядер и электронов, – это _________ энергия системы
внутренняя
внешняя
термодинамическая
потенциальная
Химическая ______________ – это изучение скорости и механизма химической реакции
______________ энтальпией (теплотой) образования химического соединения называют изменение энтальпии в процессе образования одного моля этого соединения, находящегося в стандартном состоянии, из простых веществ, также находящихся в стандартных состояниях и термодинамически устойчивых при данной температуре, фазах и модификациях
Существуют следующие типы цепных реакций: с (со) ___ цепями
неразветвленными
сходящимися
разветвленными
параллельными
Правило, гласящее, что тепловой эффект химической реакции равен сумме теплот (энтальпий) образования продуктов реакции за вычетом суммы теплот (энтальпий) образования исходных веществ, – это
правило Вант-Гоффа
следствие из закона Гесса
уравнение Аррениуса
принцип Ле Шателье
Состояние системы, при котором скорость прямой реакции равна скорости обратной реакции, – это
физическая адсорбция
химическая кинетика
химическое равновесие
хемосорбция
Энтропия изолированной системы в самопроизвольном процессе возрастает, т.е. ее изменение больше нуля, – это
второй закон термодинамики
закон действующих масс
первый закон термодинамики
закон Гесса
______________ теория позволяет рассчитывать оптимальные значения энергий связей и межатомных расстояний у реагирующих веществ и катализаторов и осуществлять выбор наилучшего катализатора
Кристаллические решетки ______________ кристаллов состоят из чередующихся положительно и отрицательно заряженных ионов, между которыми действуют электрические силы притяжения
Закон ______________ – это правило, гласящее, что тепловой эффект химической реакции не зависит от пути ее протекания, а зависит лишь от природы и физического состояния исходных веществ и продуктов реакции
Установите соответствие между понятиями и их определениями
принцип Ле Шателье
функциональная зависимость константы скорости реакции k от температуры: 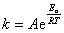
правило Вант-Гоффа
правило, гласящее, что при повышении температуры на 10о скорость большинства реакций увеличивается в 2–4 раза
уравнение Аррениуса
правило, гласящее, что если на систему, находящуюся в равновесии, оказать внешнее воздействие, то равновесие сместится в том направлении, которое ослабит эффект внешнего воздействия
______________ – это вещество, резко увеличивающее скорость реакции, но не расходующееся в результате ее протекания
Все молекулы в системе, запас энергии которых не ниже энергетического барьера реакции, находятся в особом состоянии, которое принято называть переходным или состоянием активированного ______________
Система, состоящая из двух или нескольких фаз, – это _________ система
экзотермическая
гомогенная
гетерогенная
эндотермическая
Установите соответствие между понятиями и их определениями
первый закон термодинамики
энтропия изолированной системы в самопроизвольном процессе возрастает, т.е. ее изменение больше нуля
закон действующих масс
правило, гласящее, что при постоянной температуре скорость химической реакции прямо пропорциональна произведению концентраций реагирующих веществ, взятых в степенях, равных стехиометрическим коэффициентам в уравнении реакции
второй закон термодинамики
правило, гласящее, что теплота, подведенная к системе, расходуется на увеличение ее внутренней энергии и на совершение системой работы над внешней средой
Вещество, частицы которого поглощаются поверхностью или объемом другого вещества (газ, жидкость или растворенный компонент), называют _____________
сорбатом
катализатором
сорбентом
промотором
______________ реакции – это реакции, протекающие с выделением энергии в виде теплоты в окружающую среду
Теория, объясняющая свойства твердых тел на основании анализа строения и плотности заполнения электронами энергетических зон в их кристаллах, называется ______________ теорией
Число мест, занимаемых каждым лигандом во внутренней сфере комплекса, – это
радиоактивность
электроотрицательность
координационная емкость лиганда
анизотропность
Реакции, протекающие поглощением энергии в виде теплоты из окружающей среды, – это _________ реакции
необратимые
обратимые
экзотермические
эндотермические
______________ закон термодинамики – это энтропия изолированной системы в самопроизвольном процессе возрастает, т.е. ее изменение больше нуля
При ______________ разрыве ковалентной связи образуются атомы или группы атомов (свободные радикалы) с повышенной реакционной активностью, обусловленной наличием неспаренного электрона
кинетическом
гомолитическом
гетеролитическом
каталитическом
По признаку молекулярности реакции разделяются на
экзотермические
эндотермические
мономолекулярные
бимолекулярные
тримолекулярные
Установите соответствие между понятиями и их определениями
адсорбция
сорбция объемом вещества
десорбциия
процесс отрыва частиц адсорбата от поверхности адсорбента, т.е. явление, обратное адсорбции
абсорбция
сорбция только поверхностью вещества