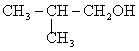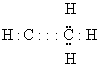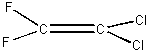Химия (школьное обучение)
В промышленности аммиак получают
взаимодействием солей аммония с щелочами
восстановлением оксидов азота водородом
соединением азота с водородом
разложением солей аммония
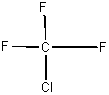
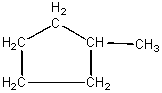
Формула 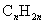 является общей молекулярной формулой соединений ряда
является общей молекулярной формулой соединений ряда
аренов
алкинов
циклоалканов
алканов
При действии на белок концентрированного раствора азотной кислоты
выпадает белый осадок
раствор приобретает желтую окраску
раствор не изменяет своего цвета
раствор приобретает голубую окраску
Растворы сульфата меди (II) и хлорида меди (II) можно различить по
взаимодействию с раствором гидроксида калия
взаимодействию с железом
взаимодействию с раствором нитрата бария
запаху
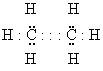
Химическая связь в молекуле азота 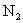
металлическая
ковалентная неполярная
ковалентная полярная
ионная
Одну молекулу бензола можно получить в процессе тримеризации
пропина
ацетилена
циклогексана
этилена
Химическая связь в молекуле аммиака 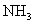
ионная
ковалентная неполярная
ковалентная полярная
металлическая
Наличие альдегидной группы в органическом веществе можно установить с помощью
гидроксида натрия
индикатора - лакмуса
аммиачного раствора Ag2O
бромной воды
Хлор может реагировать со всеми веществами, перечисленными в одном ряду
оксид меди (II), серная кислота, азот
вода, оксид серы (VI), кальций
водород, соляная кислота, кислород
вода, натрий, водород
Изомером 2-метилпропанола-1 является
2-метилбутаналь
бутандиол-1,4
бутанол-2
3-метилбутанол-1
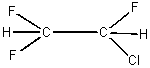
Число различных алканов, образующихся при действии металлического натрия на смесь 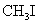 и
и 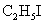 , равно
, равно
4
3
1
2
В схеме превращений С2Н2 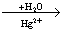 Х1
Х1 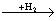 Х2
Х2 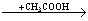 Х3 веществом Х3 является
Х3 веществом Х3 является
глицерин
ацетон
этилацетат
диэтиловый эфир
Составьте уравнение реакции алюминия с серой. Коэффициент перед формулой окислителя равен
2
3
1
4
Хлорид калия можно получить при действии хлора на следующие галогениды
Молекулярная формула алкана, плотность паров которого по воздуху равна 4,414, имеет вид
С оксидом фосфора (V) реагирует
оксид серы (IV)
кислород
оксид углерода (IV)
оксид кальция
Вещество, формула которого СН3-СН2-СООН, называется
масляной кислотой
пропионовой кислотой
уксусной кислотой
ацетальдегидом
Аминокислоты - органические вещества, в которых имеется
группа -NH2 и группа 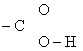
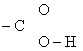
группа -NH2
группа 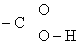
группа -NО2
Учение о пространственном строении молекул называется
биохимией
неорганической химией
квантовой химией
стереохимией
С разбавленной серной кислотой реагируют оба вещества из пары
нитрат серебра (I) и серебро
барий и сульфат бария
оксид ртути (II) и ртуть
магний и оксид меди (II)
В схеме превращений С6Н6 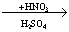 Х1
Х1 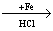 Х2 веществом Х2 является
Х2 веществом Х2 является
хлорид фениламмония
фенолят натрия
анилин
фенол
2 моль углекислого газа образуется при полном сгорании
2 моль этана
1 моль пропана
1 моль метана
1 моль этана
Формула внешнего энергетического уровня атома селена соответствует электронной конфигурации
3s23p6
4s24p4
4s24p6
3s23p4
Химическая связь в хлориде кальция
ковалентная неполярная
ионная
ковалентная полярная
металлическая
СН3ОН используется в промышленности для получения
пропаналя
этаналя
этанола
метаналя
При гидролизе метилового эфира пропионовой кислоты образуются продукты
СН3ОН и СН3СН2СН2СООН
СН3СН2СН2ОН и СН3СН2СООН
СН3ОН и СН3СН2СООН
СН3СН2ОН и СН3СН2СООН
Гидролиз жиров в технике используется для получения
этанола
синтетических моющих средств
низших кислот
мыла
При окислении пропаналя образуется
пропионовая кислота
метилэтиловый эфир
пропанол
пропиловый эфир уксусной кислоты
С раствором ортофосфорной кислоты реагируют оба вещества пары
аммиак, гидроксид калия
сера, аммиак
гидроксид меди (II), раствор хлорида натрия
серебро, нитрат серебра
В молекуле ацетилена атомы углерода находятся в состоянии
sp3-гибридизации
негибридном
sp-гибридизации
sp2-гибридизации
Жиры представляют собой
простые эфиры этиленгликоля и карбоновых кислот
простые эфиры глицерина и высших карбоновых кислот
сложные эфиры глицерина и высших карбоновых кислот
сложные эфиры этиленгликоля и карбоновых кислот
Кислоты получают
окислением альдегидов
окислением кетонов
восстановлением альдегидов
восстановлением кетонов
Конечным продуктом гидролиза крахмала является
фруктоза
глюкоза
мальтоза
глюкоза и фруктоза